
(二)影响离解平衡的因素
弱酸和弱碱的离解平衡都是暂时的、相对的动态平衡。当外界条件改变时,离解平衡像其它平衡一样,会发生移动,结果弱酸和弱碱的离解程度都有所增减。因此,可以应用平衡移动原理,通过改变外界条件,控制弱酸和弱碱的离解程度。外界条件主要指温度,同离子效应和盐效应的影响。
1.温度的影响
温度变化能使离解平衡发生移动,这种移动是通过离解常数的改变实现的,但在常温范围内变化不大。
2.同离子效应
离子浓度的改变,对弱酸和弱碱离解程度的影响极为显著。
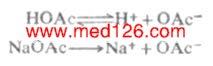
例如,在醋酸溶液中加入一些醋酸钠,由于醋酸钠是强电解质,在水溶液中完全离解Na+OAc-,这样溶液中[OAc-]增大,使
离解平衡向左移动,从而降低了醋酸的离解度和溶液中的H+浓度。
 又如,在氨水中加入一些氯化铵,由于氯化铵是强电解质,在水溶液中完全离解成NH4+和CL-,这样溶液中[NH4+]增大,使离解平衡向左移动,从而降低了氨水的离解度和溶液中的OH-浓度。
又如,在氨水中加入一些氯化铵,由于氯化铵是强电解质,在水溶液中完全离解成NH4+和CL-,这样溶液中[NH4+]增大,使离解平衡向左移动,从而降低了氨水的离解度和溶液中的OH-浓度。

由此可以得出结论,在弱电解质溶液中,加入与弱电解质具有相同离子的强电解质,使弱电解质的离解度降低的效应,称为同离子效应。
3.盐效应
在弱电解质溶液中,加入与弱电解质没有相同离子的强电解质,而使弱电解质的离解度略微增大的效应,称为盐效应。
盐效应的产生,是由于强电解质的加入,使溶液中离子间的相互牵制作用增强,离子结合成分子的机会减少,降低了分子化的程度,因而达到平衡时,弱电解质的离解度比未加入强电解质时略微大些。
例如,在0.1mol・L-1HOAc溶液中加入NaCL晶体,使NaCL的浓度为0.1mol・L-1时,[H+]不是1.32×10-3mol・L-1,而是1.70×10-3mol・L-1,离解度不是1.32%而是1.70%.
应该指出,在发生同离子效应的同时,必然伴随着盐效应的发生.这两个效应对弱电解质离解度影响不同.盐效应可以使弱电解质的离解度增大一些,而同离子效应可以使弱电解质的离解度大大降低.这说明同离子效应和盐效应对溶液酸碱性的影响是不能相提并论的.因此,对稀溶液来说,如不考虑盐效应,是不会引起很大误差的.
二、多元酸碱在溶液中的离解
多元酸碱在溶液中的离解是分步进行的,叫做分步离解。表2-2列出了一些常见的多元酸的分步离解常数。表中pKa为Ka的负对数值。
表2-2 一些常见的多元酸的分步离解常数
| 酸性强度增加 | 名称 | 分子式 | Ka1 | PKa1 | Ka2 | PKa2 | Ka3 | PKa3 |
| 草酸 | H2C2O4 | 5.4×10-2 | 1.27 | 5.4×10-5 | 4.27 | 2.2×10-13 | 12.67 | |
| 亚硫酸 | H2SO3 | 1.54×10-2 | 1.81 | 1.02×10-7 | 6.91 | |||
| 磷酸 | H3PO4 | 7.52×10-3 | 2.12 | 6.23×10-8 | 7.21 | |||
| 丙二酸 | CH2(COOH)2 | 1.38×10-3 | 2.86 | 2×10-6 | 5.70 | |||
| 邻苯二甲酸 | C6H4(COOH)2 | 1.12×10-3 | 2.95 | 3.9×10-5 | 5.41 | |||
| 酒石酸 | (CHOHCOOH)2 | 9.1×10-4 | 3.04 | 4.3×10-5 | 4.37 | |||
| 碳酸 | H2CO3 | 4.30×10-7 | 6.37 | 5.61×10-11 | 10.25 | |||
| 氢硫酸 | H2S | 9.1×10-8 | 7.04 | 1.1×10-12 | 11.96 |
例如草酸(H2C2O4)的离解分两步进行。
一级离解
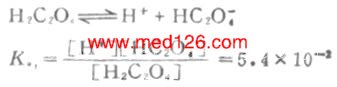
二级离解
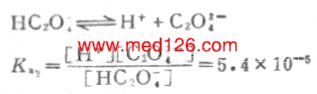 二级离解总比一级离解困难,因为H+要克服带有两个电荷的C2O2-4对它的吸引。从Ka1和Ka2可以反映这一点。草酸溶液中的HC2O-4浓度要比C2O2-4浓度大得多。
二级离解总比一级离解困难,因为H+要克服带有两个电荷的C2O2-4对它的吸引。从Ka1和Ka2可以反映这一点。草酸溶液中的HC2O-4浓度要比C2O2-4浓度大得多。
磷酸的离解要分三步,有Ka1、Ka2、和Ka3三个离解常数,且Ka1》Ka2》Ka3。这说明多元酸分级离解是依次变难。
根据多元酸的浓度和各级离解常数,可以算出溶液中各种离子的浓度。
例2 计算0.1mol・L-1H2S溶液中的H+和S2-的浓度。
解:由于H2S的 Ka1》Ka2 ,所以H2S溶液中的H+主要来自第一步离解,而第一步离解所产生的H+,又抑制第二步离解。这样计算H2S溶液中H+的总浓度时,可以忽略第二步离解的H+,近似地等于第一步离解平衡时H+浓度。
设第一步离解平衡时[H+]=x,则[H+]≈[HS-],平衡时则有下列关系:
 由表2-2知H2S的Ka为9.1×10-8,则
由表2-2知H2S的Ka为9.1×10-8,则

因Ka1很小,x必然很小,所以0.1-x≈0.1,则

溶液中的S2-是第二步离解的产生,因此,计算溶液中的S2-浓度时,应根据第二步离解平衡进行计算.
设第二步离解时,[S2-]=y,平衡时有下列关系:

因为Ka1极小,y必然极小,所以9.54×10-5±y≈9.54×10-5,则

所以,[S2-]≈Ka2。