
ЎЎЎЎГё·ЦЧУәЬҙуЈ¬ЖдҙЯ»ҜЧчУГНщНщІўІ»РиТӘХыёц·ЦЧУЈ¬ИзУГ°ұ»щлДГёҙҰАнДҫ№Пө°°ЧГёЈ¬К№ЖдлДБҙЧФN¶ЛҝӘКјЦрҪҘЛх¶МЈ¬өұЖдФӯУРөД180ёц°ұ»щЛбІР»щұ»Л®Ҫвөф120ёцәуЈ¬КЈУаөД¶МлДИФУРЛ®Ҫвө°°ЧЦКөД»оРФЎЈУЦИзҪ«әЛМЗәЛЛбГёлДБҙCД©¶ЛөДИэлД(—ұы—Лҝ—з?ЗР¶ПЈ¬УаПВІҝ·ЦТІУРГёөД»оРФЈ¬ЧгјыijЩøөДҙЯ»Ҝ»оРФҪцУлЖд·ЦЧУөДТ»РЎІҝ·ЦУР№ШЎЈ
ЎЎЎЎІ»Н¬өДГёУРІ»Н¬өД»оРФЦРРДЈ¬№К¶ФөЧОпУРСПёсөДМШТмРФЎЈАэИзИйЛбНСЗвГёКЗҫЯУРБўМеТм№№МШТмРФөДГёЈ¬ЛьДЬҙЯ»ҜИйЛбНСЗвЙъіЙұыНӘЛбөДҝЙДж·ҙУҰЈәӘӨ
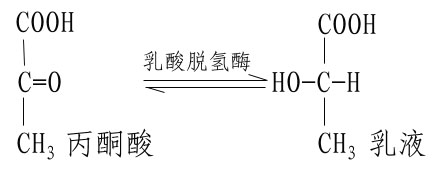
ЎЎЎЎL(+)ИйЛбНЁ№эЖдІ»¶ФіЖМјФӯЧУЙПөД—CH3Ўў—COOHј°—OH»щ·ЦұрУлИйЛбНСЗвГё»оРФЦРРДөДAЎўBј°CИэёц№ҰДЬ»щНЕҪбәПЈ¬№КҝЙКЬГёҙЯ»Ҝ¶шЧӘұдОӘұыНӘЛбЎЈ¶шD(-)ИйЛбУЙУЪ—OHЎў—COOHөДҝХјдО»ЦГУлL(+)ИйЛбПа·ҙЈ¬УлГёөДИэёцҪбәП»щНЕІ»ДЬНкИ«ЕдәПЈ¬№КІ»ДЬУлГёҪбәПКЬЖдҙЯ»Ҝ(Нј2)ЎЈУЙҙЛҝЙјыЈ¬ГёөДМШТмРФІ»ө«ҫц¶ЁУЪГё»оРФЦРРДөД№ҰДЬ»щНЕөДРФЦКЈ¬¶шЗТ»№ҫц¶ЁУЪөЧОпәН»оРФЦРРДөДҝХјд№№ПуЈ¬Ц»УРДЗР©УРТ»¶ЁөД»ҜС§Ҫб№№Ј¬ДЬУлГёөДҪбәП»щНЕҪбәПЈ¬¶шЗТҝХјд№№РНУЦНкИ«ККУҰөД»ҜәПОпЈ¬ІЕДЬЧчОӘГёөДөЧОпЎЈ
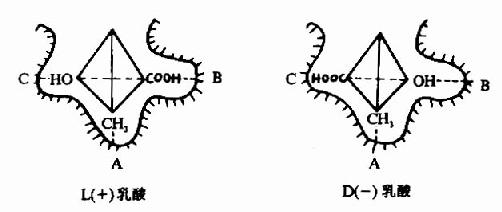
Нј2-2 ИйЛбНСЗвГёөДБўМеТм№№МШТмРФ
AЎўBЎўC·ЦұрОӘLDH»оРФЦРРДөДИэёц№ҰДЬ»щНЕ
ЎЎЎЎө«КЗЈ¬ГёөДҪб№№І»КЗ№М¶ЁІ»ұдөДЈ¬УРИЛМбіцГё·ЦЧУ(°ьАЁёЁГёФЪДЪ)өД№№РНУлөЧОпФӯАҙІў·ЗОЗәПЈ¬өұөЧОп·ЦЧУУлГё·ЦЧУПаЕцКұЈ¬ҝЙУХөјГё·ЦЧУөД№№ПуұдөГДЬУлөЧОпЕдәПЈ¬И»әуөЧОпІЕДЬУлГёөД»оРФЦРРДҪбәПЈ¬Ҫш¶шТэЖрөЧОп·ЦЧУ·ўЙъПаУҰ»ҜС§ұд»ҜЈ¬ҙЛјҙЛщОҪГёЧчУГөДУХөјЖхәПС§Лө(induced fit theory)ЎЈУГXСЬЙд·ЦОцөД·Ҫ·ЁТСЦӨГчЈ¬ГёФЪІОУлҙЯ»ҜЧчУГКұ·ўЙъБЛ№№Пуұд»ҜЎЈӘӨ
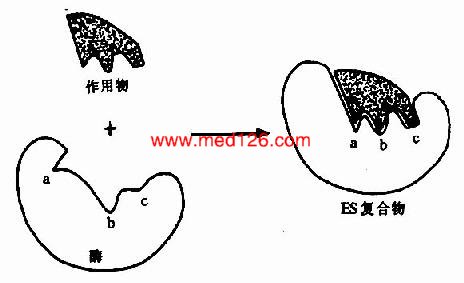
Нј2-3 өЧОпУлГёПа»ҘЧчУГөДЎ°УХөјЖхәПЎұДЈКҪНј