





| 编号 | 0276 |
| 总例数 | 117例 |
| 性别例数 | 男86例,女31例 |
| 治疗组例数 | 41例 |
| 对照组例数 | 76例 |
| 年龄区间 | 治疗组:17~58岁;对照组:19~63岁 |
| 平均年龄 | 治疗组:37.6±7.8岁;对照组:39.2±8.3岁 |
| 疾病 | 慢性乙型肝炎 |
| 并发症 | |
| 药品通用名称 | 干扰素 |
| 药品商品名称 | |
| 药品英文名称 | Interferon |
| 剂型 | 注射剂 |
| 规格 | |
| 批准文号 | |
| 生产厂家 | |
| 分类 | 生物制品 |
| 用药目的 | 治疗 |
| 用法用量 | 对照组予以干扰素α-2b每周3次肌肉注射,每次5mU/L,疗程24周。治疗组在使用上述干扰素α-2b抗病毒治疗的基础上,加用胸腺肽α1,每周2次皮下注射,每次1.6mg,疗程24周。 |
| 联合用药 | 胸腺肽α1 |
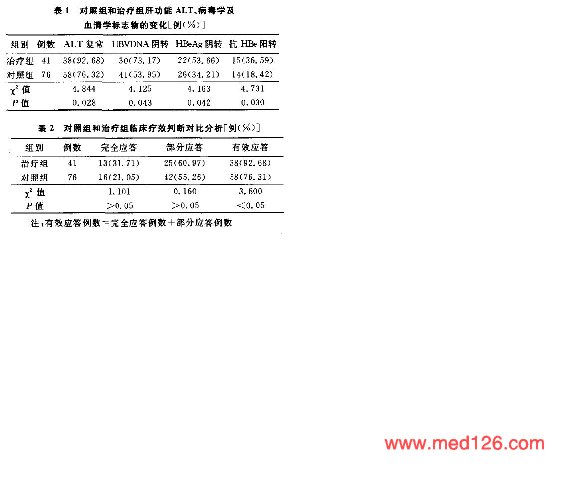
| 疗效评价标准 | ①单项生物化学应答:治疗结束时,肝功能ALT复常为有效,ALT仍异常为无效。单项病毒学应答:治疗结束时,HBVDNA转阴或血清HBVDNA 滴度较基线明显下降(下降值>1Ocopies/m1)为有效,达不到此标准为无效。单项血清学应答:治疗结束时,HBeAg阴转或HBeAg血清学转换(HBeAg阴转、抗-Hbe阳转)为有效,HBeAg仍阳性或无HBeAg血清学 转换为无效。②临床疗效判断--联合应答标准:治疗结束时,单项生物化学、病毒学以及血清学应答均有效,为完全应答;单项病毒学、血清学及生物化学应答均无 |
| 治疗效果及临床指征比较 |
 |
| 本研究报道不良反应 | |
| 其他报道不良反应 |