|
编号
|
0572
|
|
总例数
|
60例
|
|
性别例数
|
|
|
治疗组例数
|
30例
|
|
对照组例数
|
30例
|
|
年龄区间
|
35~75岁
|
|
平均年龄
|
治疗组:58.24±10.34岁;对照组:61.52±7.83岁
|
|
疾病
|
脑梗死
|
|
并发症
|
|
|
药品通用名称
|
依达拉奉
|
|
药品商品名称
|
|
|
药品英文名称
|
Edaravone
|
|
剂型
|
注射剂
|
|
规格
|
|
|
批准文号
|
|
|
生产厂家
|
|
|
分类
|
化学药品
|
|
用药目的
|
治疗
|
|
用法用量
|
观察组入院后即予依达拉奉每次30mg加入生理盐水100ml静脉滴注,2次/d,14d为1疗程。全部病例于6h内给予尿激酶)100万u溶于生理盐水100 ml静脉滴注,30 min内滴完。30 min后如肌力无改善,追加尿激酶50万u。两组患者于溶栓后均采用低分子右旋糖酐500 ml静脉滴注,1次/d,共14 d,作为基础治疗,并酌情应用甘露醇。于溶栓24 h后口服阿司匹林300mg/d,共10d,以后改为100mg/d,共80d,总疗程为90d。
|
|
联合用药
|
尿激酶
|
|
疗效评价标准
|
采用全国第四届脑血管病学术会议制定的脑卒中神经功能缺损评分标准和临床疗效评定标准,在治疗前和治疗后2 h、24 h、7 d、14 d、28 d、90 d进行评价。
|
|
治疗效果及临床指征比较
|
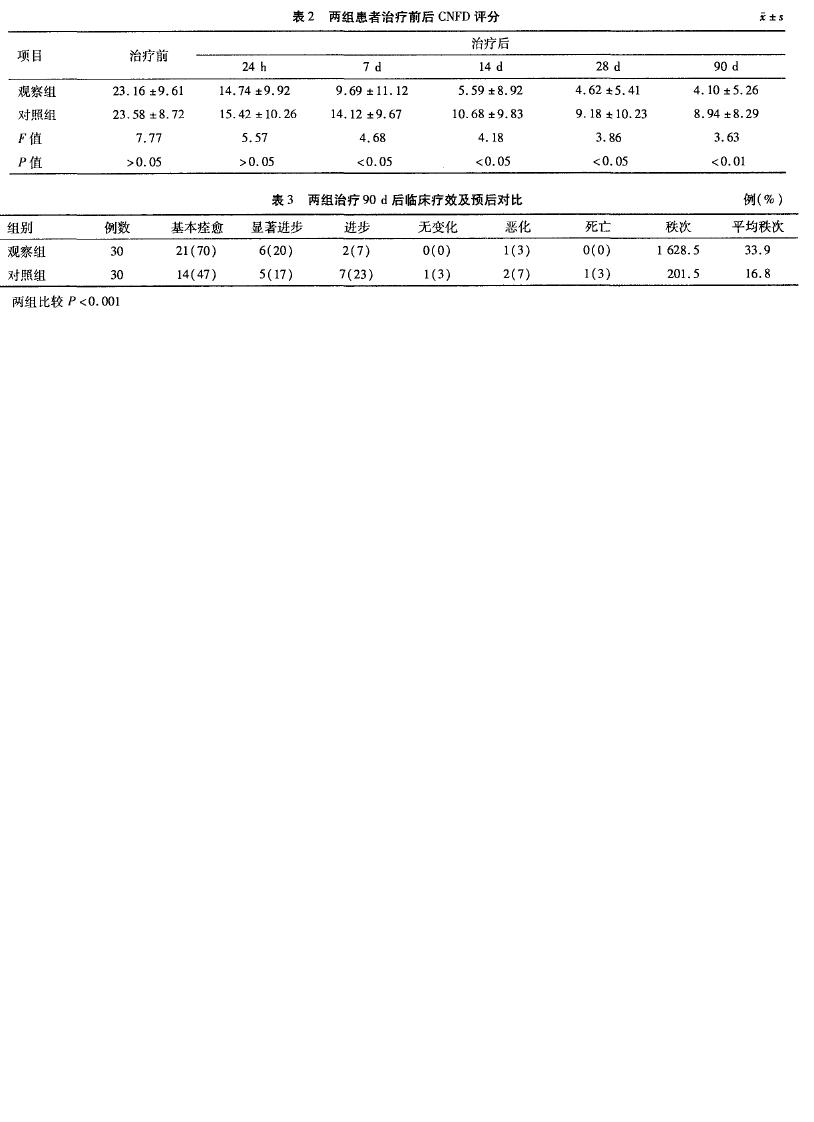
|
|
本研究报道不良反应
|
观察组副作用发生率为2/30(6.7%),表现为牙龈出血及皮疹各1例。静脉滴注依达拉奉时患者的呼吸、血压和心率无任何变化,无肝肾功能损害。对照组副作用的发生率为26.7%(8/30),出血性脑梗死2例,症状性脑出血1例,消化道出血2例,皮肤黏膜出血3例。
|
|
其他报道不良反应
|
|






