





| 编号 | 1044 |
| 总例数 | 18例 |
| 性别例数 | 男12例,女6例 |
| 治疗组例数 | |
| 对照组例数 | |
| 年龄区间 | 65~78岁 |
| 平均年龄 | 72.0±5.2岁 |
| 疾病 | 老年晚期非小细胞肺癌 |
| 并发症 | |
| 药品通用名称 | 注射用盐酸吉西他滨 |
| 药品商品名称 | |
| 药品英文名称 | Gemcitabine Hydrochloride for Injection |
| 剂型 | 粉针剂 |
| 规格 | |
| 批准文号 | |
| 生产厂家 | |
| 分类 | 化学药品 |
| 用药目的 | 治疗 |
| 用法用量 | 吉西他滨第1、8天每天、每次按体表面积800~lO00mg/m2静脉滴注定为治疗1周期,化疗前患者均用枢丹8rag静脉注射作止吐预处理,3周后重复上述治疗。每例完成2周期治疗后作评价。 |
| 联合用药 | |
| 疗效评价标准 | 按1981年WHO制订的实体瘤癌近期评价标准分为完全缓解(CR)、部分缓解(PR)、无变化(NC)、进展(PD);有效率=CR PR。生存期:从化疗开始至死亡或末次随访时间。 |
| 治疗效果及临床指征比较 | 18例患者共完成68周期治疗,平均3.7周期。PR 33.3%(6/18),NC 27.8%(5/18),PD37.8%(7/18),有效率为33.3%。生存期2~18个月,中位生存期7~8个月。 |
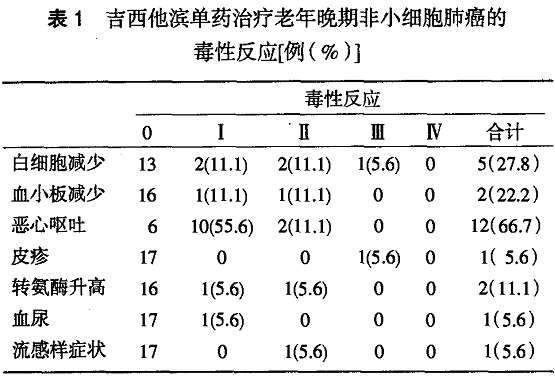
| 本研究报道不良反应 |
 |
| 其他报道不良反应 |