|
编号
|
100
|
|
总例数
|
86例
|
|
性别例数
|
男51例,女37例
|
|
治疗组例数
|
60例
|
|
对照组例数
|
28例
|
|
年龄区间
|
治疗组:43~82岁;对照组:44~81岁
|
|
平均年龄
|
治疗组:61.3岁;对照组:60.6岁
|
|
疾病
|
脑梗死
|
|
并发症
|
|
|
药品通用名称
|
藻酸双酯钠
|
|
药品商品名称
|
脉洛畅
|
|
药品英文名称
|
Alginic Sodium Diester Injection
|
|
剂型
|
注射剂
|
|
规格
|
|
|
批准文号
|
|
|
生产厂家
|
山西亚宝药业
|
|
分类
|
化学药品
|
|
用药目的
|
治疗
|
|
用法用量
|
治疗组:应用脉洛畅150mg溶于生理盐水250ml中静滴,2O~4O滴/min,1次/d,14d为1个疗程 对照组:应用维脑路通注射液0.4g溶于生理盐水25Oml中静滴,2O~40滴/min,1次/d,14d为1个疗程。
|
|
联合用药
|
|
|
疗效评价标准
|
临床疗效参照1995年第四届全国脑血管病学术会议通过的脑卒中患者临床神经功能缺损程度评分标准评定:基本治愈:临床神经功能缺损程度评分(NFD)减少91%~100%,病残
程度0级;显著进步:NFD减少46%~9O%,病残程度1~3级Ⅰ进步:NFD减少18%~45%;无变化:NFD减少或增加17%以内;恶化:NFD增加18%以上;死亡。
|
|
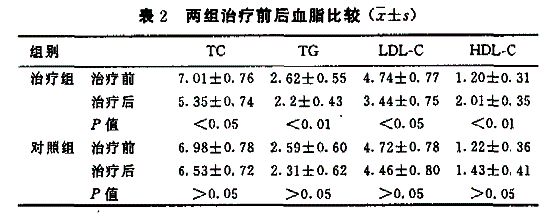
治疗效果及临床指征比较
|


|
|
本研究报道不良反应
|
治疗组:2例出现轻度头痛,1例出现恶心、呕吐,均于减慢滴速后症状消失。对照组:1例出现头痛、头晕,3例出现心悸、胸闷,均于减量后症状消失。
|
|
其他报道不良反应
|
|








