





| 编号 | 82 |
| 总例数 | 90例 |
| 性别例数 | 男58例,女32例 |
| 治疗组例数 | 90例 |
| 对照组例数 | 0例 |
| 年龄区间 | |
| 平均年龄 | (48±5.6)岁 |
| 疾病 | 2型糖尿病 |
| 并发症 | 合并糖尿病神经病变20例,糖尿病肾病12例,糖尿病酮症68例,合并肝功能损害6例,合并糖尿病眼底病变12例。 |
| 药品通用名称 | 30/70混合重组人胰岛素 |
| 药品商品名称 | 甘舒霖30R |
| 药品英文名称 | 30/70 Mixture Recombinant Human Insulin |
| 剂型 | 注射剂 |
| 规格 | |
| 批准文号 | |
| 生产厂家 | 吉林通化东宝药业股份有限公司 |
| 分类 | 生物制品 |
| 用药目的 | 治疗 |
| 用法用量 | 随机分成两组,A组用甘舒霖30/70,B组用诺和灵30R,早晚餐前30分钟皮下注射,联合应用阿卡波糖(拜唐苹或卡博平),监测血糖(空腹及三餐餐后),调整胰岛素剂量,总疗程为3个月,疗程结束复查FBG、2hBG、HbAlc、腰围、体重、计算体重指数,并记录低血糖发生次数和胰岛素用量,两组治疗前年龄、体重、血糖均无统计学差异。 |
| 联合用药 | |
| 疗效评价标准 | |
| 治疗效果及临床指征比较 |
(1)两组降糖效果比较(见表1)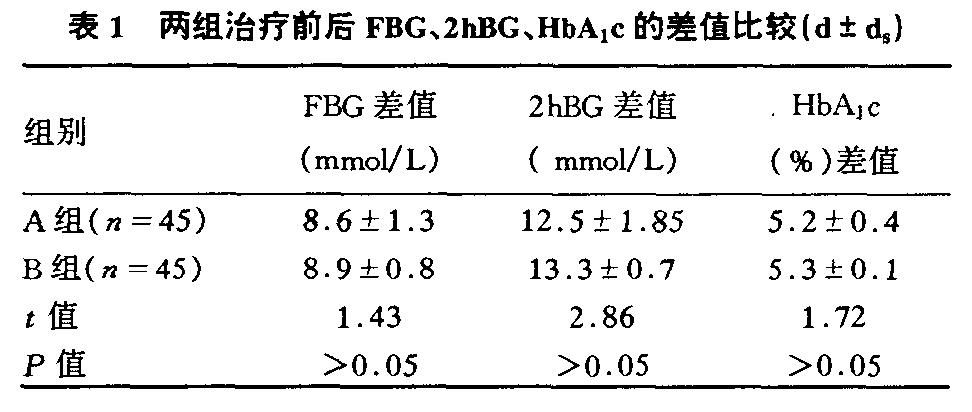 ,从上表看出,两组治疗后FBG、2hBG、HbA1C的差值经统计,P>0.05,说明A组和B组的治疗效果无差异。(2)两组治疗后BMI、腰围均有所上升,但无统计学意义(P>0.05),胰岛素用量比治疗初期减少(表2) 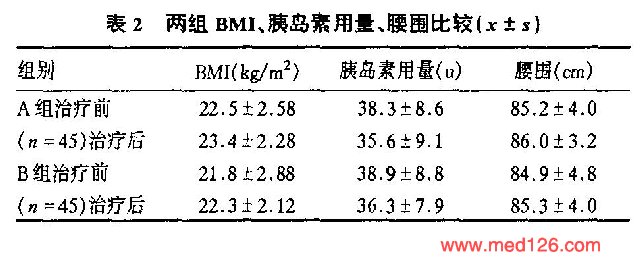 。 |
| 本研究报道不良反应 | 低血糖发生次数为A组8人次,B组9人次。且大多数为中餐前发生,过敏反应A组5人次(均为皮下硬结,可耐受),B组3人次,但有1例发生过敏反应(全身起水疱)而停用。 |
| 其他报道不良反应 |