





| 编号 | 242 |
| 总例数 | 80例 |
| 性别例数 | 男43例,女37例 |
| 治疗组例数 | 42例 |
| 对照组例数 | 38例 |
| 年龄区间 | |
| 平均年龄 | 治疗组(38±12)岁;对照组(37±10)岁 |
| 疾病 | 糖尿病酮症酸中毒 |
| 并发症 | |
| 药品通用名称 | 生物合成人胰岛素 |
| 药品商品名称 | 诺和灵R |
| 药品英文名称 | Biosynthetic Human Insulin |
| 剂型 | 注射剂 |
| 规格 | 100U/ml |
| 批准文号 | |
| 生产厂家 | 丹麦诺和诺德公司 |
| 分类 | 生物制品 |
| 用药目的 | 治疗 |
| 用法用量 | CSⅡ组采用生物合成人胰岛素(丹麦诺和诺德公司生产100U/m1)经海创胰岛素泵通过连接导管及皮下埋置针头昼夜不停地输入基础胰岛素,如进餐则可在进餐时输入餐前追加量,全天胰岛素用量为每小时每公斤体重0.1U,其中50%为基础量,50%为餐前追加量,可平均分配于三餐前,或按4:3:3的比例分别分配于三餐前,应用罗氏血糖仪监测末梢血糖值,根据血糖值调整基础胰岛素量及三餐前追加胰岛素量;若患者无法进食,则输注5%葡萄糖液或葡萄糖盐水,生物合成人胰岛素用量改为按输入的葡萄糖与胰岛素的比例计算,一般可根据病人血糖情 |
| 联合用药 | |
| 疗效评价标准 | 血糖达标:空腹血糖<6.1mmol/L,餐后2小时血糖<8.0mmol/L。血糖≤3.0mmol/L,无论有无症状均定义为低血糖。 |
| 治疗效果及临床指征比较 |
治疗后两组空腹血糖均较治疗前明显下降(P<0.01),但治疗后两组空腹血糖比较,差异无统计学意义(P>0.05),见表1 。治疗后CSⅡ组胰岛素用量为每日(41±8)U,常规组胰岛素用量为每日(48±6)U,两组比较差异有统计学意义(P<0.01);CSⅡ组血糖达标时间、尿酮体转阴时间和血酮体达标时间均较常规组明显缩短,差异有统计学意义(P<0.05),见表2 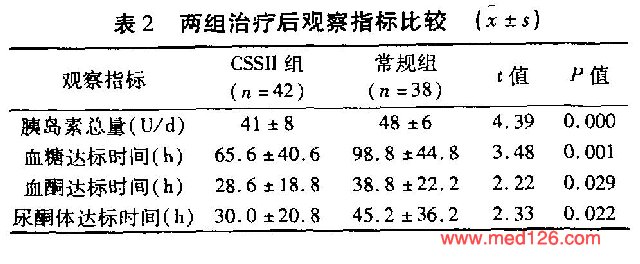 。CSⅡ组低血糖发生率为2.4%(1/42 |
| 本研究报道不良反应 | |
| 其他报道不良反应 |