





| 编号 | 438 |
| 总例数 | 106例 |
| 性别例数 | 男58例,女48例 |
| 治疗组例数 | 56例 |
| 对照组例数 | 50例 |
| 年龄区间 | |
| 平均年龄 | 治疗组(41.3±7.2)岁;对照组(39.2±6.7)岁 |
| 疾病 | 1型糖尿病、2型糖尿病 |
| 并发症 | CSⅡ组(A组)合并酮症l5例,合并感染6例,合并糖尿病肾病8例,合并糖尿病视网膜病变3例,合并糖尿病周围神经病变3例。MSⅡ组(B组)合并酮症11例,合并感染7例。 |
| 药品通用名称 | 生物合成人胰岛素 |
| 药品商品名称 | 诺和灵R |
| 药品英文名称 | Biosynthetic Human Insulin |
| 剂型 | 注射剂 |
| 规格 | |
| 批准文号 | |
| 生产厂家 | 诺和诺德公司 |
| 分类 | 生物制品 |
| 用药目的 | 治疗 |
| 用法用量 | 治疗组(A组)用瑞士产H-TRONP1US-V100型胰岛素泵持续皮下输注胰岛素,胰岛素应用诺和诺德公司产诺和灵R,每日胰岛素总量按公斤体重(0.6±0.2)IU给予,将每日胰岛素总量的50%设为基础量,余量按20%、15%、15%分配作为三餐前负荷量,并根据血糖水平酌情调整胰岛素剂量。对照组(B组)于每日三餐前皮下注射诺和灵R和睡前皮下注射诺和灵中效胰岛素。 |
| 联合用药 | |
| 疗效评价标准 | 两组病人的血糖控制目标均为空腹血糖3.9~8.3mmol/L,餐后两小时血糖3.9~10.1mmoL/L。 |
| 治疗效果及临床指征比较 |
两组一般情况的比较:A(治疗)、B(对照)两组病人在年龄、性别、病程、体重指数(BMI)、糖化血红蛋白(HbAlc)方面差异均无统计学意义(P>0.05)。详见表1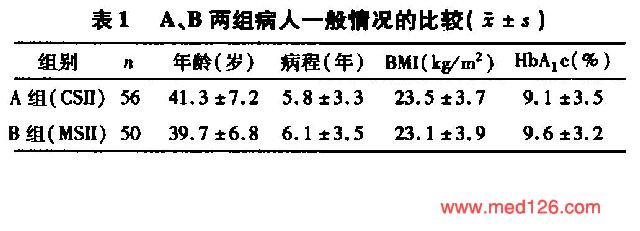 。两组治疗效果的比较:A、B两组病人在用胰岛素强化治疗后血糖均达到控制目标。A组血糖平均达标时间短于B组(P<0.01);平均每日胰岛素用量A组明显少于B组(P<0.05),详见表2  。 |
| 本研究报道不良反应 | A组(治疗组)仅出现1人次低血糖反应,B组(对照组)出现9人次低血糖反应。 |
| 其他报道不良反应 |