





| 编号 | 1452 |
| 总例数 | 60例 |
| 性别例数 | |
| 治疗组例数 | 30例 |
| 对照组例数 | 30例 |
| 年龄区间 | |
| 平均年龄 | |
| 疾病 | 2型糖尿病 |
| 并发症 | |
| 药品通用名称 | 那格列奈 |
| 药品商品名称 | |
| 药品英文名称 | Nateglinide |
| 剂型 | 片剂 |
| 规格 | 30mg |
| 批准文号 | |
| 生产厂家 | 那格列奈片:军事医学科学院药物毒物研究所研制 |
| 分类 | 化学药品 |
| 用药目的 | 治疗 |
| 用法用量 | 服药方法:① 清洗期:试验前服用口服降糖药的患者停止用药,开始2周的清洗期,此期间继续饮食/运动控制;②随机双盲治疗期:清洗期过后,试验组接受12周的那格列奈片120,一天三次治疗,对照组接受瑞格列奈片1mg,一天三次治疗。均为每餐前15分钟口服,不进餐不服药。 |
| 联合用药 | |
| 疗效评价标准 | 治疗12周后,FBG值及2 hPBG与基础值相比下降30% 为显效,10%~29%为有效,无变化或低于10%为无效。 |
| 治疗效果及临床指征比较 |
60名受试者中52人完成全部14周的试验(含2周平衡期),其中7人(试验组4人,对照组3人)因不能按期完成随访或不能遵守试验方案而中途退出研究,试验组有1例因不良反应(低血糖反应)退出研究。经过12周治疗后,2组药物在降低FBG及PBG疗效方面具有一致性,试验组降低FBG有效率56%,降低2 hPBG有效率80.00%;对照组降低FBG有效率76.92%,降低2 hPBG有效率73.08%。2组差异无显著性意义(P>0.05),见表1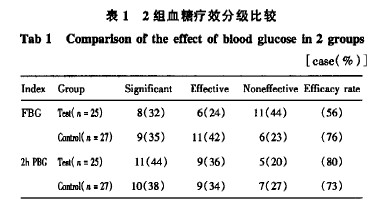 。经过12周 |
| 本研究报道不良反应 | 在试验期间无严重不良事件发生。试验组与研究药物有关的不良事件发生2例(6.67%),其中导致脱落的不良事件为1例;对照组2例(6.67%),无导致脱落的不良事件发生。2组相比较差异无统计学意义。其中那格列奈不良事件 主要包括:皮疹1例,消化不良1例。瑞格列奈不良事件包括:低血糖反应2例。2组低血糖反应发生率相比无显著性差异,出现反应者均较快自行恢复,以后的随访中未检测出低血糖。 |
| 其他报道不良反应 |