 打印本文
打印本文  关闭窗口
关闭窗口 物理化学(1)
一、判断题(10分)
1、在绝热过程中,环境对体系作功,则体系的温度必定升高,内能减少。
2、一封闭体系的绝热循环过程必为一可逆循环过程。
3、在恒定温度、压力下,反应 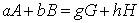 ,达到化学平
,达到化学平
衡的条件是 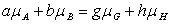 。
。
4、所有化学反应,在开始反应时的速率都是最大的,以后逐步减小。5、分散相微粒半径大于入射光波长是发生光散射现象的必要条件。
6、光化反应中光起催化剂作用,因此又叫光催化反应。
7、电解质对溶胶的聚沉能力常用聚沉值表示,若某电解质的聚沉值越大,则其聚沉能力越强。
8、二组分完全互溶溶液和气相平衡共存时,易挥发组分在气相中的含量大于它在液相中的含量。
9、在任何温度下,氢电极的标准电极电势均为零。
10、化学反应的速率可用产物或反应物浓度随时间的变化率来表示。
二、选择题(30分)
1、对于相变过程,
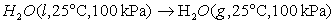 ,
,
可用来判断其方向的是( )
① △S孤 和 △US,V ② △GT,P 和 △F T,V
③ △HS,P 和 △G T,P ④ △S孤 和 △G T,P
2、1mol N2(g)与2mol O2(g),在等温、等压下混合,若它们都为理想气体,则混合过程熵变△Smix为( )J•K-1
① 3.8 ② 0
③ 15.88 ④ 0.29
3、在一定温度下,0.2mol A(g)与0.6mol B(g)进行下列反应:
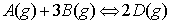
当增加体系压力时,反应的标准平衡常数Kθ( );A的转化率αA( )
① 变大 ② 变小
③ 不变 ④ 无一定变化规律
4、1mol某理想气体,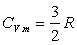 ,由337℃,400 kPa的始态变为337℃,200 kPa的终态,此过程的△G( );△F( )
,由337℃,400 kPa的始态变为337℃,200 kPa的终态,此过程的△G( );△F( )
① ﹥0 ② ﹤0
③ = 0 ④ 无法确定
5、在等温等压下,以可逆方式将单位面积的固体浸润在液面上时,其吉布斯能变化为( )
① ΔG = σ固-液 – σ气-液 ② ΔG = σ气-固 – σ液-固
③ ΔG = σ气-液 – σ气-固 ④ ΔG = σ液-固 + σ气-液
6、溶胶的聚沉速度与ζ电位的关系是( )
① ζ电位愈大,聚沉愈快 ② ζ电位愈正,聚沉愈快
③ ζ电位为零,聚沉最快 ④ ζ电位愈负,聚沉愈快
7、一个反应的活化能为83.68 kJ•mol-1,在室温27℃时,温度每增加1K,反应速率常数增加的百分数为( )。
① 4% ② 90% ③ 11% ④ 50%
8、基元反应A+B→P+…的活化能Ea=100 kJ•mol-1,在定容条件下,50℃、初始浓度CA,0 = CB,0 = a mol•dm-3时,测得其半衰期为t1/2,在100℃、初始浓度仍然相同时,测得的半衰期为t’1/2,则( )。
① t’1/2 < t1/2 ② t’1/2 = t1/2
③ t’1/2 > t1/2 ④ 无法确定
9、反应CH3CHO→CH4+CO,其活化能为190 kJ•mol-1,当加入催化剂碘蒸汽后,活化能降为136 kJ•mol-1,若加入催化剂后,反应的频率因子不变,则在500℃时加入催化剂后反应速率增大( )倍。
① 2.3×10-6 ② 4.38×10 5
③ 4.46×10 3 ④ 2.24×10-4
10、绘制乙醇-水-氯苯相图实验中,每次以水滴定,体系由清液变白色混浊,即意味着( )。
① 反应到达终点,生成沉淀物质
② 体系由单液相区进入固相区
③ 体系由单液相区进入两液相区
④ 体系由液相区进入固相区
 打印本文
打印本文  关闭窗口
关闭窗口